滴定实验是贯穿Alevel化学的核心考点,其中 AS阶段涉及题型均能达到 9分左右的大分值,由于其涵盖运算和表述部分,具有一定综合性,也是部分考生容易失分的一环。实际上,酸碱中和滴定实验,是用已知浓度的酸 (或碱)通过滴加的方式,结合指示剂的颜色变化临界点与酸碱物质的量关系以确定待求碱 (或酸)浓度的常用实验方法。本篇将由理综教研部老师从操作步骤、运算方法与实验仪器等多个维度来具体讲解这一高分值模块的作答方式。
高分模块
综合精讲
『过程表述』
对滴定过程的描述,理综教研部要求考生理解记忆对应关键词:润洗器皿、滴定管与移液管的使用、添加指示剂、滴定终点附近逐滴添加、重复实验获得稳定滴定值。具体过程描述可参考:
1)Rinsetheglasswarewithdistilledwaterandappropriatesolutions注:锥形烧瓶只以蒸馏水进行润洗,移液管和滴定管先后用蒸馏水以及各自待称量的液体进行润洗。锥形烧瓶若以待盛液体润洗,会导致待测溶液测算浓度偏大
2)Filltheburettewith… (solutionA),ensuringtherearenoairbubbles or gap inthetip
3)Usepipette (andpipettefiller)totransfer25 of… (solutionB)toa conical flask
of… (solutionB)toa conical flask
4)Add … (indicator) to the conical flask and carry out a rough/trail titration注:首次滴定仅获取滴定差值的大致范围
5)Add … (solutionA)dropbydropneartheendpoint and swirl before each drop to ensure the complete reaction,until the indicator just changes color
6)Repeattitrationsuntilconcordanttitresareobtained
『仪器相关』
1、pipette:用于移取特定体积的液体
1)润洗:先后用蒸馏水 (distilledwater)和待测液体进行润洗。注:如果只用蒸馏水进行润洗,移液管内的液体会被稀释,对应的滴定差值也会变小;滴定管同理若只以蒸馏水润洗会导致滴定差值偏大2)在滴定过程中,少量液体残留在移液管尖,可视为预留的容错空间,无需将这部分残余液全部转移到烧瓶中。注:若将残余液体全部转移至烧瓶中,反而会导致滴定差值偏大
2、burette:用于移取所需体积未知的液体,以使用前后的读数差 Vinitial-Vfinal来确定使用的液体体积
在滴定管的使用过程中有如下注意事项:

来源:理综教研部化学 U2讲义截图
『指示剂选择』
在化学 2中,考生需掌握两种指示剂的颜色变化:
1)酚酞 (phenophthalein):遇碱变粉、在酸性和中性时无色。
2)甲基橙 (methylorange):遇酸变红、遇碱变黄、中性时为橙色。
对于 methyl orange,不管是酸滴入碱还是碱滴入酸,endpoint处均为橙色。
在判断 endpoint处的颜色变化时,理综教研部温馨提示一定要判断清楚是酸滴入碱、还是碱滴入酸。找准题目中是否有以下描述:
“pipette…A…intoconicalflask”即“用 pipette称量的 A液体被滴定”,则是另一液体 B滴入 A
“filltheburettewith…B…”即“用 burette称量的 B液体为滴定剂”,则是 B滴入另一液体 A
“(…A…)titratedwith…B…”中“titratedwith”后跟着的是滴定剂,则是 B滴入 A
 来源:2021年 10月化学 U2真题卷
来源:2021年 10月化学 U2真题卷
注: 虽为盐类,但其溶液呈碱性
虽为盐类,但其溶液呈碱性
比如:以 HCl (aq)作为滴定剂,对 (aq)进行滴定,methylorange作为指示剂,则溶液在 endpoint处颜色变化为:yellowtoorange。另外,若问到为何不选用某种指示剂时,可考虑溶液本身颜色或反应中的颜色变化是否会干扰指示剂的颜色显示。
(aq)进行滴定,methylorange作为指示剂,则溶液在 endpoint处颜色变化为:yellowtoorange。另外,若问到为何不选用某种指示剂时,可考虑溶液本身颜色或反应中的颜色变化是否会干扰指示剂的颜色显示。
『数据处理』
1、待测液体的浓度计算
酸碱中和实验的整体计算逻辑为: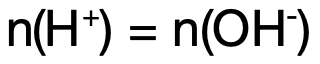
因此:
若标准液的体积、浓度已知,待测液的体积已知,即可用上述等式计算出待测液体的浓度。要特别注意方程中酸、碱前的系数,如果是一元酸和二元碱反应、二元酸和一元碱反应,计算摩尔数时注意乘以 2或 1/2。在计算初始样本的质量或摩尔数时,理综教研部尤其强调最后一步需乘上对应的体积倍数,这一步也是考生容易出现错漏的一步。
比如在下图呈现的真题中,该考生以n=cv计算得出的摩尔数,是在单次滴定中添加的 HCl的摩尔数,根据方程中反应物的系数之比,有 n(MOH) =n(HCl) = 0.00512mol,也就是 25.0 MOH溶液的摩尔数,而在 Step 2中,把金属 M溶于水得到的 MOH溶液共有 250
MOH溶液的摩尔数,而在 Step 2中,把金属 M溶于水得到的 MOH溶液共有 250 ,每次滴定都是取了总溶液的 1/10,因此摩尔数需要乘10,才是 n(totalMOHin250
,每次滴定都是取了总溶液的 1/10,因此摩尔数需要乘10,才是 n(totalMOHin250 )。
)。
 来源:理综教研部模拟作答过程图
来源:理综教研部模拟作答过程图
2、meantitre运算
平均滴定值的运算一般也是滴定运算中的第一步,一定不要掉以轻心,部分考生在计算这一步时出现错误,则导致后面相关小问连错。在滴定数据的选择上,需选取 concordanttitres,即数据之间差值在 0.20 以内的,才纳入计算。简答题中所有对滴定值进行取舍的原因,都可以从“concordanttitre”这一角度考虑。
以内的,才纳入计算。简答题中所有对滴定值进行取舍的原因,都可以从“concordanttitre”这一角度考虑。
 来源:理综教研部教材滴定实验术语截图
来源:理综教研部教材滴定实验术语截图
理综教研部尤其强调对于“concordanttitre”这一概念的关注,以下是整合的一些常见提问与参考作答:
Q:“Whytitre2andtitre4shouldbediscarded?”
A:“Titre2andtitre4arenotconcordant(with other titres) .”
Q:“Why should thefirsttitrebediscarded?”
A:“Titre1 is not concordant (with other titres).”/“Titre1isarangefinder.”
Q:“Whyfurthertitrationisnotnecessary?”
A:“Concordant titres have been obtained.”
 来源:2019年 10月化学 U2真题卷
来源:2019年 10月化学 U2真题卷
3、percentageuncertainty的计算
用误差值除以实际称量值,转换为百分比形式即为测量误差的计算。注:pipette读数只读一次,误差值只需乘 1;而 burette都需读数两次 (Vinitial-Vfinal),因此误差值需乘2
例:用移液管 (pipette)移取 15 的液体,每次读数误差为 0.05
的液体,每次读数误差为 0.05 ,则 percentageuncertainty=
,则 percentageuncertainty= × 100% = 0.333%;用滴定管 (burette)滴加 15
× 100% = 0.333%;用滴定管 (burette)滴加 15 的液体,每次读数误差为 0.05
的液体,每次读数误差为 0.05 ,先后两次读数误差叠加则 percentageuncertainty=
,先后两次读数误差叠加则 percentageuncertainty= ×100% = 0.667%
×100% = 0.667%
4、purity的计算
purity= ×100%
×100%
样品总质量一般为题目中的给定数据,其中包含杂质质量;而该物质的实际质量需要通过反应方程式、通过已知产物的化学量进行计算。以上就是本篇理综教研部针对 Alevel化学中滴定实验的归纳解析,助力攻下高分值题型,欢迎各位反复阅读,熟悉内化才是关键。预祝各位在接下来的一月统考赛季中能够稳步摘星,大跨步奔赴梦校。